den 9 januari 2023
Ny metod hittar rätt behandling till bröstcancerpatienter
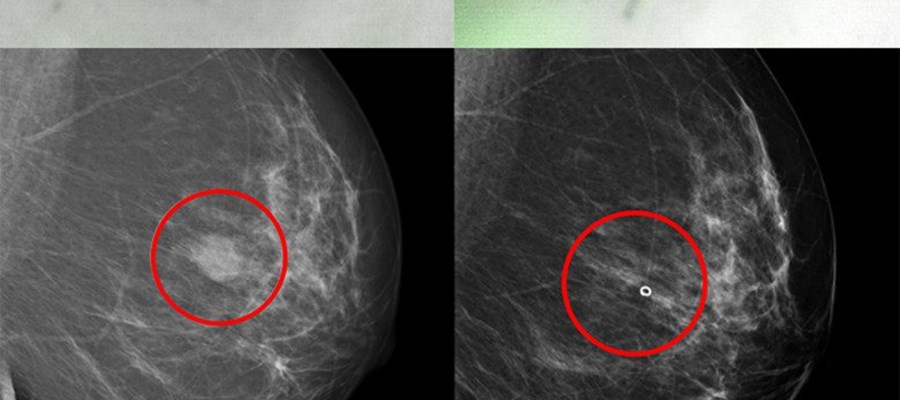
Forskare vid Karolinska Institutet har utvecklat en metod som ska kunna förutsäga om en patient med bröstcancer kommer att ha nytta av en viss behandling eller inte. Den cellbaserade metoden har testats på patienter med lovande resultat, enligt en studie som publiceras i PNAS.

Johan Hartman
Professor vid Karolinska Institutet. Foto: Stefan Zimmerman.

Xinsong Chen
Forskningsspecialist vid Karolinska Institutet. Foto: Niklas Elmehed.
– Idag finns begränsade möjligheter att på förhand säga vilka bröstcancerpatienter som har nytta av olika behandlingar. Den här metoden kan förutsäga hur patienterna kommer att svara på vissa behandlingar, vilket gör att man kan undvika onödiga biverkningar och spara kostnader. Det behövs större bekräftande studier, men vi ser att konceptet fungerar, säger Johan Hartman, professor vid institutionen för onkologi- patologi, Karolinska Institutet, och studiens sisteförfattare.
Idag finns flera olika läkemedel tillgängliga vid behandling av bröstcancer. Men sjukdomen är komplex och alla patienter blir inte hjälpta av samma eller alla läkemedel. Viss information om vilken behandling en patient kommer att ha nytta av går att få genom exempelvis DNA-sekvensering. Men i många fall går det inte att säga om en behandling kommer att hjälpa den individuella patienten eller inte, och därför behövs bättre metoder för att förutsäga patienternas behandlingssvar.
Den metod KI-forskarna har utvecklat bygger på att isolera och odla inte bara tumörceller utan även så kallade stödjeceller från patienter med bröstcancer. Därefter testas cancerbehandlingar i olika koncentrationer på de odlade cellerna för att se hur känsliga de är mot läkemedlen.
Cellmodellerna liknar patienternas tumörer
I den aktuella studien visar forskarna att det är praktiskt möjligt att etablera den här typen av cellbaserade tumörmodeller från brösttumörer, och att cellmodellerna liknar patienternas ursprungstumörer på relevanta sätt, till exempel genetiskt och vad gäller olika proteinmarkörer.
Tumörmodellerna skapades från biopsier från 98 patienter som opererats för bröstcancer och testades på över 35 existerande bröstcancerläkemedel och bröstcancerläkemedel under utveckling. Forskarna kunde se att den läkemedelskänslighet tumörmodellernas visade i hög grad överensstämde med känsligheten hos den tumörtyp patienterna hade, och att tumörmodellerna i vissa fall var känsliga för läkemedel under utveckling.
Därefter undersökte forskarna hur träffsäker metoden är när det gäller att förutsäga behandlingssvar. Detta gjordes på 15 bröstcancerpatienter som fick behandling innan operation, så kallad neoadjuvant behandling, vid Södersjukhuset i Stockholm.
Från biopsier tagna innan operationerna skapade forskarna tumörmodeller från varje patient och utsatte dem för samma läkemedel som patienten fick. Därefter jämfördes modellernas läkemedelskänslighet med patienternas behandlingssvar.
Hög träffsäkerhet
Resultaten visar att de behandlingssvar tumörmodellen förutsade i hög grad överensstämde med patientens behandlingssvar. Till exempel hade cytostatikan epirubicin en träffsäkerhet på 90 procent i modellen, medan fyra av fyra patienter som behandlades och testades för anti-HER2 monoklonala antikroppsläkemedel uppvisade överensstämmelse.
Forskarna poängterar att det går att skapa cellmodellerna även från små tumörer, som vanligtvis anses tekniskt svåra att odla från, och att testerna går relativt snabbt att genomföra.
– Vi kan i de flesta fall utföra individanpassad läkemedelstestning och få resultatet inom tio dagar, vilket tyder på att den här metoden kan fungera i den kliniska vardagen. Men den kan också användas inom forskning och läkemedelsutveckling, säger studiens försteförfattare Xinsong Chen, forskningsspecialist vid institutionen för onkologi-patologi, Karolinska Institutet.
Nästa steg är nu att testa metoden i större patientmaterial och att undersöka möjligheten att kombinera den med andra molekylära metoder för att förutsäga behandlingssvar ännu bättre och studera resistensmekanismer.
Källa: Karolinska Institutet
Publikation
”Breast cancer patient-derived whole-tumor cell culture model for efficient drug profiling and treatment response prediction”, Xinsong Chen, Emmanouil G. Sifakis, Stephanie Robertson, Shi Yong Neo, Seong-Hwan Jun, Le Tong, Apple Tay Hui Min, John Lövrot, Roxanna Hellgren, Sara Margolin, Jonas Bergh, Theodoros Foukakis, Jens Lagergren, Andreas Lundqvist, Ran Ma och Johan Hartman, Proceedings of the National Academy of Sciences (PNAS), 26 december, 2022, doi: 10.1073/pnas.2209856120
Forskningen är finansierad av Cancerfonden, Bröstcancerförbundet, Region Stockholm, Radiumhemmets forskningsfonder och Vetenskapsrådet. Johan Hartman är medgrundare av och delägare i Stratipath som utvecklar metoder för AI-baserade beslutsstöd för cancerdiagnostik. Företaget har dock ingen koppling till den aktuella studien. Vissa av forskarna har utanför denna studie mottagit ersättningar från läkemedelsbolag. Se den vetenskapliga studien för ytterligare information.