den 9 december 2024
Ny forskning avslöjar två typer av fettlever
Forskare vid Karolinska Institutet och Göteborgs universitet har identifierat två typer av metabolt orsakad fettlever – en leverspecifik typ och en systemisk typ som påverkar andra vävnader och organ. Upptäckten kan leda till förbättrad diagnostik och behandling av denna växande patientgrupp. Två studier har publicerats parallellt i tidskriften Nature Medicine.

Stefano Romeo
Professor. Foto: Johan Wingborg.
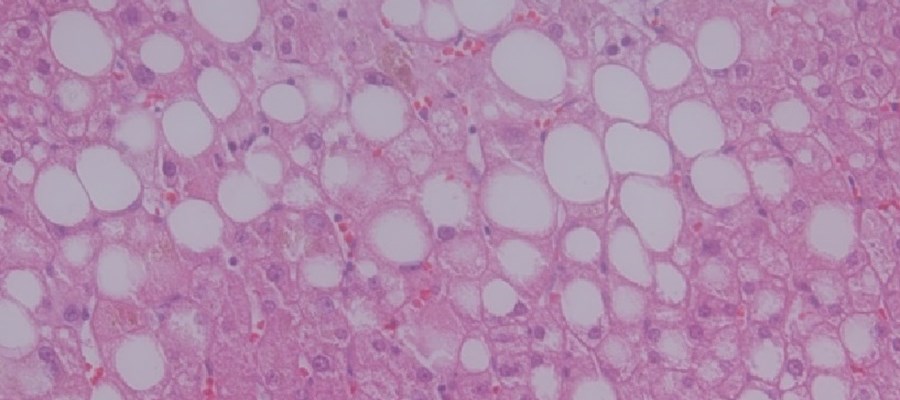
Metabolt orsakad fettlever (MASLD) kännetecknas av en överdriven fettansamling i levern, vilket kan leda till allvarlig leverskada som skrumplever (cirros) och levercancer. MASLD orsakas av övervikt och obesitas och är en stor och växande börda globalt. Man räknar med att en av fyra vuxna i världen är drabbade, men de flesta vet inte om det eftersom det ger symtom först vid framskriden sjukdom.
Omfattande analyser
Forskare vid Karolinska Institutet och Göteborgs universitet har nu identifierat två olika typer av MASLD genom att analysera data från över 36 000 deltagare från UK Biobank och från andra studier.
– Vi upptäckte att det finns minst två typer av MASLD med olika kliniska förlopp. Den ena är mer aggressiv och påverkar främst levern, medan den andra är sammankopplad med hjärta/kärl, njurar och metabola syndromet, säger Stefano Romeo, professor vid institutionen för medicin, Karolinska Institutet, som lett forskningen.
Förutsäga sjukdomsförlopp
Forskarna använde genetiska tester för att identifiera 27 nya genetiska varianter som är kopplade till MASLD. Genom att analysera dessa gener kunde de fastställa två olika riskpoäng relaterade till de två typerna av sjukdomen. Den leverspecifika typen är mer aggressiv och kan leda till allvarlig leverskada men skydda mot hjärt-kärlsjukdom, medan den systemiska typen innebär en högre risk för diabetes, hjärt-kärlsjukdom, hjärt- och njursvikt.
– Den här upptäckten är viktig eftersom den hjälper oss att förstå varför vissa individer utvecklar allvarligare leversjukdomar medan andra drabbas av hjärt- och njursjukdomar. Detta gör att vi bättre kan förutse hur dessa sjukdomar kommer att utvecklas och skräddarsy behandlingen efter patientens specifika behov, förklarar Stefano Romeo.
Två parallella studier
Tillsammans med forskare vid Université de Lille i Frankrike har Stefano Romeo kunnat visa liknande resultat genom att använda en annan metod, så kallad oövervakad klustring.
– Arbetet med klustring med hjälp av enkla kliniska variabler är av yttersta vikt eftersom det gör det möjligt för oss att på individnivå skilja ut vilka som har MASLD och kommer att utveckla hjärt-kärlsjukdom och vilka som inte kommer att göra det, säger Stefano Romeo. Klusterprognosen kan tas fram med hjälp av enkel kalkylator.
Precisionsmedicin
Studien belyser också vikten av genetisk forskning för att förstå komplexa sjukdomar som MASLD och de mekanismer som orsakar det kardiovaskulära-renala-metabola syndromet.
– Dessa två studier är ett steg framåt mot precisionsmedicin, där behandlingar skräddarsys för att passa individuella behov baserat på genetisk och klinisk information., Det kan också öka medvetenheten om hur genetik och miljöfaktorer påverkar vår hälsa och understryker vikten av fortsatt forskning inom detta område, avslutar Stefano Romeo.
Publikationer:
Oveis Jamialahmadi, Antonio De Vincentis, Federica Tavaglione, Francesco Malvestiti, Ruifang Li-Gao, Rosellina M. Mancina, Marcus Alvarez, Kyla Gelev, Samantha Maurotti, Umberto Vespasiani-Gentilucci, Frits Richard Rosendaal, Julia Kozlitina, Päivi Pajukanta, François Pattou, Luca Valenti & Stefano Romeo, Nature Medicine, online 9 december 2024, doi: 10.1038/s41591-024-03284-0.
Violeta Raverdy, Federica Tavaglione, Estelle Chatelain, Guillaume Lassailly, Antonio De Vincentis, Umberto Vespasiani-Gentilucci, Sami F. Qadri, Robert Caiazzo, Helene Verkindt, Chiara Saponaro, Julie Kerr-Conte, Gregory Baud, Camille Marciniak, Mikael Chetboun, Naima Oukhouya-Daoud, Samuel Blanck, Jimmy Vandel, Lisa Olsson, Rima Chakaroun, Viviane Gnemmi, Emmanuelle Leteurtre, Philippe Lefebvre, Joel T. Haas, Hannele Yki-Järvinen, Sven Francque, Bart Staels, Carel W. Le Roux, Valentina Tremaroli, Philippe Mathurin, Guillemette Marot, Stefano Romeo & François Pattou, Nature Medicine, online 9 december 2024, doi: 10.1038/s41591-024-03283-1.
Forskningen har huvudsakligen finansierats av Cancerfonden, Vetenskapsrådet, ALF-medel, Hjärt-Lungfonden, Knut och Alice Wallenbergs Stiftelse samt Novo Nordisk Fonden. Flera potentiella intressekonflikter anges i artikeln. Stefano Romeo har varit konsult för AstraZeneca, GSK, Celgene Corporation, Ribo-cure AB och Pfizer under de senaste fem åren och har mottagit ett forskningsanslag från AstraZeneca.
Källa: Karolinska Institutet.