den 19 maj 2025
Ny forskning om ALS öppnar för tidig behandling

Med hjälp av gensaxen CRISPR och stamceller har forskare vid Stockholms universitet och Kings College London lyckats identifiera en gemensam nämnare för olika genmutationer som alla orsakar nervsjukdomen ALS. Forskningen visar att det uppstår ALS-kopplad dysfunktionalitet i nervcellernas energifabriker mitokondrierna, innan cellerna visar andra tecken på sjukdom, något som inte tidigare varit känt. Studien publicerades nyligen i den vetenskapliga tidskriften Nature Communications.

Eva Hedlund
Professor. Foto: Sören Andersson.
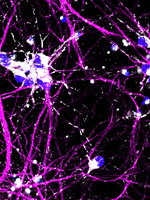
Lila nervceller med mitokondrier
Bild: Melanie Leboeuf.
– Vi visar att de nervceller som slutligen kommer att dö i ALS får problem strax efter att de bildats. Det tidigaste tecknet på problemet såg vi i cellens energifabriker, mitokondrierna * , och även i hur de transporteras ut i nervcellernas utskott där det finns ett stort behov av dem och den energi de producerar, säger Eva Hedlund, professor i neurokemi vid Stockholms universitet och ansvarig för studier.
Forskarteamet kunde slå snabbt att dessa problem var gemensamma för flera olika ALS-orsakade mutationer, något som kommer att bli betydelsefullt vid framtida behandlingar av sjukdomen.
– Det betyder att det finns en del faktorer som man skulle kunna åtgärda läkemedel mot någon sjukdom, säger Eva Hedlund.
Omprogrammerad cell
Forskarna använde gensaxarna CRISPR/Cas9 för att introducera olika ALS-orsakande mutationer i mänskliga stamceller, kallade iPS celler * . Från dem framställdes sedan motorneuroner, de nervceller som dör i ALS, samt interneuroner, nervceller som är relativt motståndskraftiga mot sjukdomen. Därefter analyseras dessa med singel cell RNA-sekvensering, en metod som gör det möjligt att identifiera alla budbärarmolekyler (mRNA) i individuella celler och därmed förstå hur de fungerar, hur de pratar med sina grannar och om de börjar få problem.
– I den data vi fick fram identifierade vi en gemensam sjukdomssignatur tvärs över alla ALS-orsakande mutationer, som var unika för motorneuroner och alltså inte uppstod i motståndskraftiga celler, säger Eva Hedlund.
Detta skedde mycket tidigt och var helt oberoende av sjukdomsframkallande muterade proteiner (FUS, eller TDP-43) fanns på fel ställe i cellen eller inte. Hittills har man trott att det är förändringen, misslokaliseringen *, i proteinerna som sker först, säger Eva Hedlund.
Banbrytande upptäckt
Inom ALS talar man ofta om att visa problem orsakas av en förlust av funktionen hos ett protein som är muterat, medan andra problem uppstår på grund av motsatsen, nämligen uppkomsten av en ny toxisk funktion som har erhållit genom mutationen, men det har enligt Eva Hedlund inte alltid varit lätt att bena ut hur det verkligen ligger till och mycket är fortfarande okänt.
– Genom att göra olika CRISPR-mutationer i den ALS-orsakande FUS-genen, har vi nu för första gången kunnat visa att de fel som uppstår orsakas av en ny toxisk egenskap hos proteinet, inte av en förlust av funktion, säger Eva Hedlund.
Cellernas energifabriker påverkas
En tredje upptäckt forskarteamen gjorde var att transporten av mitokondrier ut i axonerna * , nervcellernas utskott, där de flesta mitokondrier i nervceller behövs, var radikalt påverkad i ALS linjerna. Även detta var oberoende av de sjukdomsframkallande proteinerna fanns på fel ställe i cellen eller inte.
– Ett faktum som innebär problem eftersom det finns ett stort behov av dessa energifabriker ute i axonerna. Utan dem har nervcellerna inte nog med energi för att kunna kommunicera som de ska med andra celler, säger Eva Hedlund.
De nya upptäcktsbehandlingarna öppnar för nya tidiga metoder, något som forskarteamet fortsätter att lägga grunden för.
– Vi vill förstå hur dessa tidiga fel uppstår i känsliga nervceller i ALS, hur det påverkar energinivåer i cellerna samt deras kommunikation och nödvändiga kontakt med muskelfibrer. Vi tror att det är en mycket viktig nyckel till att förstå varför kontakten mellan motorneuroner och muskler bryter i sjukdomen och till att identifiera nya mål för terapeuter, säger Eva Hedlund.
Om ALS
Den dödliga sjukdomen ALS karaktäriseras av att nervceller i vår hjärna och ryggmärg, så kallade motorneuroner, som styr all vår skelettmuskulatur i kroppen dör och detta ledder till att musklerna bryter ner. I de flesta fall av ALS uppstår sjukdomen sporadiskt men i 10–20 procent av fallen är det olika genmutationer som orsakar sjukdomen. Det har hittills varit okänt om olika mutationer orsakar ALS på samma sätt. Det har även varit okänt varför vissa nervceller är känsliga medan andra är motståndskraftiga.
Läs mer om ALS: https://www.socialstyrelsen.se...
Några viktiga termer
* iPSCs är omprogrammerade celler som isolerats från en vuxen människas vävnader för att vändas tillbaka i utvecklingen till celler som påminner om embryonala stamceller.
* Mitokondrier är små strukturer som finns i alla våra celler. De brukar kallas cellens kraftverk; i dem förbränns socker och fett till vatten och koldioxid. Den energi som då frigörs lagras i en molekyl, ATP, som används i olika cellprocesser.
* Axoner är det utskott som nervceller skickar ut för att kontakta andra celler. I motorneurons fall så är det muskelfibrer som ska kontaktas, som ibland är över en meter bort.
* Mislokalisering betyder att något hamnar på fel stället. I ALS och även andra neurodegenerativa sjukdomar ser man felveckade proteiner på platser där proteinet normalt inte ska befinna sig.
Artikel i Nature Communications: https://doi.org/10.1101/2023.0..
Källa: Stockholms universitet.