den 10 november 2023
Första patienten behandlad med genterapin ROCTAVIAN ° (valoctocogene roxaparvovec) för svår hemofili A
Den första patienten i världen utanför kliniska studier har nu handlats med ROCTAVIAN. ROCTAVIAN är en intravenös engångsbehandling och den första genterapi som godkänts i Europa för behandling av svår hemofili A hos vuxna patienter. Underlag för hälsoekonomisk utvärdering och pris har skickats in till myndigheter i Sverige och Finland och förberedelserna är i gång för Norge och Danmark, för att möjliggöra tillgången i Norden.

Jan Astermark
Överläkare och professor.
EU-kommissionen godkände BioMarins ROCTAVIAN, den första genterapin för behandling av vuxna med svår hemofili A, i augusti 2022. Nu har en vuxen patient med svår hemofili A för första gången någonsin behandlats med ROCTAVIAN på Behandlingscenter för hemofili (HTC) i Tyskland.
”Det här är en viktig milstolpe inom hemofili och för hemofilipatienter och läkare runt om i världen som efterfrågar tillgång till behandlingen. Vi ser fram emot att fler patienter i resten av Europa nu får tillgång till Roctavian”, säger Jeff Ajer, Executive Vice President och Chief Commercial Officer på BioMarin.
Behandlingscenter för hemofili i Tyskland (HTC) screenar personer med hemofili för att besluta om de har möjlighet att behandlas med genterapin. Innan påbörjad behandling bedöms eventuella patienter kliniskt och genomgår en rad tester. För närvarande screenar HTC ett tiotal patienter parallellt med att slutgiltiga prisförhandlingar pågår i Tyskland.
”Bördan som svår hemofili A innebär för människor som lever med sjukdomen är betydande, och det finns fortfarande ett stort behov av nya effektiva behandlingsalternativ. EU-godkännandet av genterapin och möjligheten till engångsinfusion utgör en viktig milstolpe inom hemofilivården och ger nytt hopp för lämpliga patienter i såväl Norden som globalt, patienter som kan antas uppnå en större frihet utan bördan av regelbundna profylaktiska behandlingar under några år”, säger Jan Astermark, professor vid Klinisk koagulationsmedicin och ställföreträdande prefekt vid Institutionen för translationell medicin, Lunds universitet.
Förutom i Tyskland, fortsätter företaget sitt arbete mot myndigheter för att göra genterapin tillgänglig i de nordiska länderna samt i flertalet andra europeiska länder.
Hemofili A, även kallad FVIII-brist eller klassisk hemofili, är en X-kromosombunden genetisk sjukdom som orsakas av att FVIII, ett koagulationsprotein, saknas eller är defekt1. Även om sjukdomen ärvs från föräldrar till barn orsakas ungefär en tredjedel av fallen av en spontan mutation, en ny mutation som inte är nedärvd.1 Cirka 1 av 10 000 personer har hemofili A.2
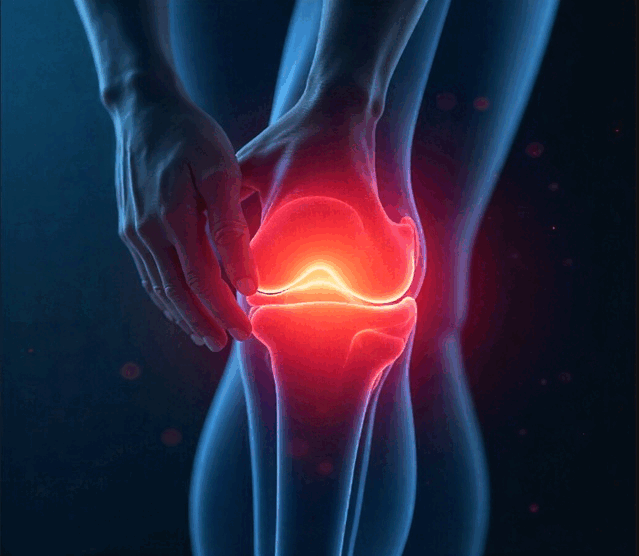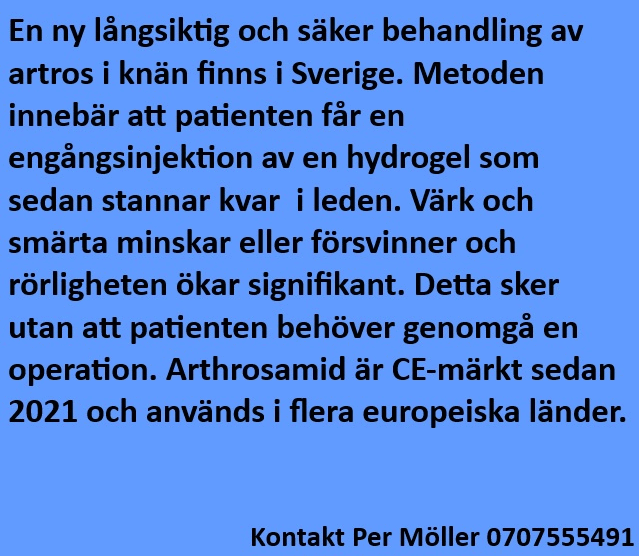
Symtom på hemofili är att man lätt får blåmärken, långvarig blödning efter ett sår, blödningar i muskler och leder samt spontanblödningar, där blödningar plötsligt uppstår i kroppen utan någon tydlig orsak.3 Personer med svår hemofili (faktornivåer som är mindre än 1 % av vad som förväntas hos en frisk person) upplever ofta smärtsamma, spontana blödningar i muskler eller leder.4 För patienter som fortsätter att drabbas av spontana blödningar kan tillståndet vara livshotande.4
De som lever med svår hemofili behöver vanligtvis intravenösa infusioner 2–3 gånger per vecka för att upprätthålla målnivåerna av koagulationsfaktorer5,6, och många har svårt att klara av denna tidskrävande rutin.7 Även med nyare icke-faktorersättningsbehandlingar kan subkutana injektioner fortfarande krävas en gång i veckan, två gånger i månaden eller en gång i månaden beroende på patienten.6,7
Trots behandling fortsätter många personer med hemofili att uppleva mikroblödningar i sina leder, vilket orsakar progressiv skada över tid.8,9 Detta är extremt smärtsamt och kan leda till att människor inte kan delta i dagliga aktiviteter, lider av depression eller ångest och lever ett liv där smärta är ett konstant inslag.3,4,10
ROCTAVIAN är avsett för behandling av svår hemofili A (medfödd faktor VIII-brist) hos vuxna patienter utan anamnes på antikroppar mot koagulationsfaktor VIII och utan detekterbara antikroppar mot adenoassocierat virus av serotyp 5 (AAV5). Engångsinfusionen fungerar genom att den tillför en funktionell gen som är utformad för att kroppen själv ska kunna producera FVIII, vilket minskar behovet av kontinuerlig profylax, vilket framgår av resultat som rapporterats under en 3-årig studieperiod.
Europeiska kommissionen (EC) beviljade Roctavian villkorat marknadsgodkännande den 24 augusti 2022. ° Detta läkemedel är föremål för utökad övervakning.
Referenser:
- National Bleeding Disorders Foundation. Hemophilia A. https://www.hemophilia.org/bleeding-disorders-a-z/types/hemophilia-a. Last accessed September 2023.
- Makris M et al. The European Haemophilia Network (EUHANET). Blood Transfus 2014;12(Suppl 3):s515-s518.
- World Federation of Hemophilia. Hemophilia. Available at: https://elearning.wfh.org/elearning-centres/hemophilia/. Last accessed September 2023.
- O’Hara J et al. The cost of severe haemophilia in Europe: the CHESS study. Orphanet Journal of Rare Diseases;2017;12:106.
- Srivastava A et al. Guidelines for the management of Hemophilia. Haemophilia 2013;19(1):e1-47.
- Mahlangu J et al. Emicizumab prophylaxis in patients who have hemophilia A without inhibitors. N Engl J Med 2018;379:9.
- Callaghan MU et al. Long-term outcomes with emicizumab prophylaxis for hemophilia A with or without FVIII inhibitors from the HAVEN 1-4 studies. Blood. 2021;137(16):2231-2242.
- duTreil S. Physical and psychosocial challenges in adult hemophilia patients with inhibitors. J Blood Med 2014;5:115-22.
- Manco-Johnson M et al. Prophylaxis versus episodic treatment to prevent joint disease in boys with severe hemophilia. N Engl J Med 2007;357:535-44.
- O’Hara J et al. Associated impact of activity impairment on clinical and patient-centric outcomes in severe hemophilia. Haemophilia 2018;24:1.
Källa: BioMarin Nordic.